- Dénutrition Pédiatrique Orale ou Entérale
- Dénutrition Adulte Orale ou Entérale
- Polyhandicap
La nutrition de l’enfant atteint de polyhandicap : évaluer, diagnostiquer et agir
- Pédiatre
- Médecin Généraliste
- Neurologue
- Diététicien
- Gastroentérologue
Il nous manque vos centres d’intérêts pour profiter au mieux de votre expérience personnalisée
(D’après la communication du Dr Pierre Poinsot, Lyon)
La nutrition de l’enfant atteint de polyhandicap : évaluer, diagnostiquer et agir
La nutrition de l’enfant atteint de polyhandicap s’inscrit dans une prise en soin multidisciplinaire élargie : neurologie, gastroentérologie, pneumologie, kinésithérapie, médecine de réadaptation… où qualité des soins, adaptation et préservation de la qualité de vie sont des points d’attention majeurs.
L’insécurité et les difficultés alimentaires liées aux fausses routes, aux repas interminables ou à l’épuisement de l’enfant peuvent conduire à une insuffisance des apports caloriques, puis à la dénutrition. À l’inverse, certains patients peuvent être suralimentés ou en surpoids, à cause d’apports nutritionnels excédant leur besoin nutritionnel et/ou à cause de leur faible mobilité.
Lors de la journée DayNutri à Lyon le 24 février 2026, les Drs Frédéric Valla et Pierre Poinsot ont présenté une approche pratico-pratique d’une prise en soin en nutritionnelle raisonnée de l’enfant atteint de polyhandicap afin d’adapter son alimentation et de l’optimiser à chaque étape de sa vie. L’enjeu n’est pas de viser un idéal mais de s’adapter à chaque patient, chaque situation clinique et réalité de vie.
1) Comment se définit le polyhandicap ?
Toutes les définitions concernant le polyhandicap, les maladies neuromusculaires, les paralysies cérébrales... ne sont pas toujours claires même si tous ces patients ont des problématiques communes. En France, le « polyhandicap » a été défini par le décret du 9 mai 2017 comme « Les personnes présentant un dysfonctionnement cérébral précoce ou survenu au cours du développement, ayant pour conséquence de graves perturbations à expressions multiples et évolutives de l'efficience motrice, perceptive, cognitive et de la construction des relations avec l'environnement physique et humain, et une situation évolutive d'extrême vulnérabilité physique, psychique et sociale »1. Ce terme « polyhandicap » ne s’est pas imposé dans la littérature internationale. On retrouve ainsi, dans les publications anglo-saxonnes, une appellation proche avec « Profound Intellectual and Multiple Disabilities » (PIMS) qui correspond à des troubles profonds du développement intellectuel et à une déficience motrice grave1. Au final, comme l’a expliqué le Dr Frédéric Valla, le polyhandicap est donc une affection neurologique acquise dès la naissance ou dans les 3 premières années de vie. Il aura des conséquences importantes liées à des perturbations graves à expressions multiples et évolutives. Il y aura toujours une déficience intellectuelle profonde, avec des altérations de la communication et de la régulation émotionnelle, avec souvent des troubles sensoriels et toujours, avec une déficience motrice grave. Sur le plan nosologique, on peut distinguer un continuum au sein de la paralysie cérébrale (PC), qui regroupe l’IMC et l’IMOC. L’IMC correspond à une infirmité motrice cérébrale avec atteinte motrice sévère, sans déficience intellectuelle. L’IMOC désigne une infirmité motrice d’origine cérébrale associant une déficience motrice sévère à une déficience intellectuelle légère à modérée. Le polyhandicap, en revanche, constitue une situation différente, caractérisée par l’association de déficiences motrices et intellectuelles sévères. Lors d’un diagnostic différentiel, il est possible de distinguer les multi-handicaps avec le pluri-handicap qui associe de deux à plusieurs déficiences, sans déficience intellectuelle (ex : la surdi-cécité) ou le sur-handicap où le handicap est ici la conséquence d’un handicap initial.
Quelques chiffres à retenir (faire un encadré)
En France, la prévalence du polyhandicap est d’environ 0,5 pour 1 0001. L’étiologie est identifiée dans 70 à 80 % des situations : causes prénatales dans 65 à 80 % des cas (souvent génétiques, incluant des maladies neurologiques évolutives), périnatales dans 10 à 15 % (en particulier la grande prématurité) et post-natales dans 10 à 15 %. La médiane de survie est de 58 ans (IC95 % : 55,5-60,5) selon les données de la cohorte française EVAL-PLH 2, la première cause de décès étant la décompensation respiratoire par surinfection bronchique.
2) Quels sont les défis de l’alimentation chez l’enfant atteint de polyhandicap ?
Chez l’enfant atteint de polyhandicap, l’alimentation est souvent mise en difficulté à cause de plusieurs mécanismes concomitants tels que des troubles posturaux, dentaires, de la déglutition et de la digestion. L’issue clinique peut s’avérer délétère et conduire à des complications infectieuses et pulmonaires graves lorsqu’un de ces maillons de la chaîne nutritionnelle est mal contrôlée4.
Un des premiers facteurs aggravants sont les troubles posturaux, dont principalement la scoliose. Ils interfèrent fréquemment avec la déglutition et la prise orale, tout en ayant un retentissement respiratoire et digestif. De même, dans certains contextes post-chirurgicaux de scoliose, un syndrome de pince aorto-mésentérique entraîne des complications pouvant entraver la progression digestive et accélérer la dénutrition. Un autre paramètre sont les troubles dentaires3. Souvent sous-estimés, ils méritent une attention soutenue. Des douleurs oro-faciales, une mauvaise hygiène buccale, la stase salivaire retentissent sur le bon déroulement de la prise alimentaire en limitant la mastication et augmentant le risque de fausse route. Une consultation odontologique devrait ainsi être réalisée régulièrement.
Focus sur la déglutition
La dysphagie est corrélée à la sévérité du déficit moteur. Sa prévalence atteint 90 à 99 % des patients avec 8 % de formes modérées, 76 % de formes modérées à sévères et 15 % de dysphagie totale4. Les conséquences sont à la fois nutritionnelles (baisse des ingesta, dénutrition), organisationnelles (temps de repas prolongés) et respiratoires (fausses routes, pneumopathies d’inhalation).
Afin d’assurer la sécurité alimentaire, l’évaluation de ce trouble doit être minutieuse L’observation d’un repas doit rechercher des signes de fausse route directs (toux) ou indirects (voix encombrée). De plus, l’utilisation de la radio-cinéma de déglutition4 s’avère très utile pour documenter la coordination pharyngée, les aspirations silencieuses, les résidus intrabuccaux, une déglutition retardée, la cinétique du larynx et la corrélation symptômes/imagerie. Par contre, la manométrie haute résolution semble plus discutable car invasive mais elle peut permettre de préciser une dysmotilité œsophagienne, notamment lors de tableaux cliniques confus.
Focus sur le reflux gastro-oesophagien (RGO)
Le RGO4, très fréquent, est d’origine multifactorielle à cause de relaxations inappropriées du sphincter inférieur de l’œsophage, de la diminution de la clairance œsophagienne, de la dysmotricité avec diminution du péristaltisme et/ou de retard de vidange gastrique. La pression intra-abdominale se trouve ainsi fréquemment augmentée et le décubitus limite l’effet de la gravité sur la clairance œsophagienne. Certains médicaments comme les benzodiazépines peuvent aussi aggraver les RGO4.
Les complications sont principalement digestives, respiratoires et nutritionnelles. Une toux post-prandiale et un RGO externalisé sans effort de vomissement sont des indicateurs clés. Le diagnostic des RGO est donc avant tout clinique et complété, au besoin, par une pHmétrie, parfois couplée à l’impédancemétrie. De plus, une gastroscopie peut être préconisée en cas de signes d’œsophagite.
La prise en charge des RGO s’avère donc multiple. Les règles hygiéno-diététiques de prévention en privilégiant une bonne posture et des repas fractionnés par exemple, peuvent aider le patient ; et la kinésithérapie respiratoire avant le repas vise à réduire les efforts de toux post-prandiale.
Des traitements médicamenteux, tels que les inhibiteurs de la pompe à protons peuvent être prescrits de façon transitoire. Ils modifient peu le volume du reflux et ne préviennent pas les aspirations. Leurs effets indésirables à long terme doivent être anticipés (infections pulmonaires et digestives, malabsorption, ostéopénie)4. Dans les formes sévères, la question d’un abord jéjunal (gastro-jéjunostomie) peut s’inscrire dans une stratégie de protection des voies aériennes et de contrôle des symptômes (reflux sévère, et gastroparésie).
Focus sur la constipation
La constipation est fréquente et multifactorielle4. Sa prévention repose sur trois piliers : la posture/mobilisation, l’apport hydrique entérale adéquat et l’apport en fibres (par voie orale ou entérale). Les laxatifs osmotiques sont souvent nécessaires. Une tachyphylaxie au long cours, dans environ 50 % des cas, oblige une stratégie graduée et une réévaluation régulière. Dans des situations spécifiques, des suppositoires ou des lavements peuvent être discutés. Les fibres alimentaires doivent être considérées comme un outil de régulation4. Leur introduction doit être progressive, corrélée à l’hydratation et réévaluée en fonction des ballonnements, douleurs ou épisodes diarrhéiques. Dans le cadre d’une nutrition entérale, choisir une formule avec fibres permet d’améliorer le transit en adaptant les volumes hydriques.
3) Comment réaliser et consolider une bonne évaluation nutritionnelle ?
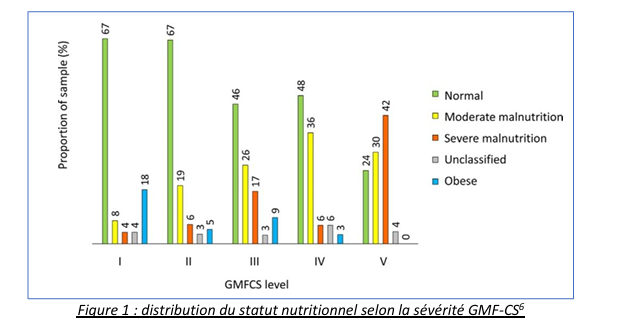
L’augmentation de la malnutrition sévère est corrélée à la sévérité du handicap selon la classification GMF-CS (Gross Motor Fonctionnal Classification System)5. Ainsi, les adaptations stratégiques nutritionnelles sont essentielles afin d’ajuster la nutrition à la sévérité et à l’évolution des enfants atteints de polyhandicap.
Les besoins énergétiques de ces jeunes patients peuvent énormément variés et sont dépendants de leur mobilité, de leurs troubles physiologiques/posturaux et de leurs infections (figure 1)6. Il faut noter que le risque de surnutrition est fréquent, l’obésité, généralement de la masse grasse tronculaire, est présente dans 8 % des cas6. Viser un IMC (indice de masse corporelle) plus bas qu’un enfant du même âge sans handicap (22/23) est à privilégier afin de faciliter la prise en charge par les aidants et limiter les surcharges pondérales.
L’équilibre nutritionnelle n’est pas donc uniforme, surtout lors de la croissance des enfants, et doit être ré-évaluer régulièrement. Chez un enfant très sarcopénique, la priorité sera la densité calorico-protéique. Chez un enfant peu mobile avec adiposité tronculaire, la qualité de la composition corporelle nutritionnelle et la prévention des complications métaboliques seront à favoriser, sans jamais compromettre la sécurité de la déglutition.
L’évaluation en pratique
Les évaluations doivent être répétées, standardisées et régulières7. Les étapes peuvent se schématisées par des mesures anthropométriques (poids, taille, périmètre brachial) tous les 6 mois, une estimation de la masse grasse par pli tricipital tous les 6 mois, un bilan biologique carentiel annuel et une exploration de la composition corporelle par DEXA environ tous les 2 ans.
La mesure de la taille se fera souvent de façon manière indirecte et imprécise (ex : longueur Talon-Genou, Longueur Tibiale, longueur Ulnaire), avec une variabilité de plus ou moins 5 cm7. Il est donc important d’utiliser toujours la même méthode de mesure. Des courbes de croissance spécifiques, notamment selon le niveau GMF-CS, ont été proposées dans des cohortes à forte incidence de dénutrition. Les recommandations ESPGHAN confirment l’efficacité d’utiliser les courbes nationales, avec un objectif de poids entre le 10e et le 25e percentile8, tout en individualisant les conclusions en fonction du tonus, de la mobilité, des comorbidités du jeune patient.
Les critères de dénutrition
Comme vu ci-dessus, chez l’enfant atteint de polyhandicap, la dénutrition ne se lit pas sur une valeur isolée mais sur sa cinétique. Le suivi régulier des courbes de poids et de taille impose de comparer les trajectoires et d’utiliser strictement la même méthode de mesure au fil du temps. Chez l’enfant atteint de polyhandicap, la présence d’un seul des critères HAS de dénutrition doit immédiatement faire évoquer un risque de dénutrition. En effet, les critères HAS de dénutrition ont été pensés pour le patient adulte et ceux-ci ne sont pas transposables chez l’enfant atteint de polyhandicap pour des raisons physiologiques, métrologiques et cliniques4. Les critères sont les suivants :
Si un seul de ces critères est présent, l’enfant atteint de polyhandicap peut souffrir de dénutrition. Son alimentation doit être adaptée immédiatement.
Remarque : L’association Ressources Polyhandicap Hauts-de-France a réalisé des fiches pdf en accès libre qui apportent de nombreuses informations sur l’état nutritionnel. A télécharger gratuitement sur https://ressourcespolyhandicap.org/wp- content/uploads/2021/11/8-Etat-Nutritionnel.pdf
Les besoins nutritionnels
Les besoins énergétiques sont dépendants de nombreux facteurs dont l’état musculaire et infectieux. Des mesures calométriques indirectes (mode Canopy) apportent de précieuses informations sur les besoins caloriques en fonction de la présence ou non de masse maigre, bien qu’elles ne soient pas facilement réalisables au quotidien. L’estimation des besoins énergétiques chez l’enfant atteint de polyhandicap repose donc d’abord sur la dépense énergétique au repos (DER), calculée à partir des équations de Schofield. Ces valeurs doivent être ajustées car ces patients présentent fréquemment un hypométabolisme relatif, largement lié à la réduction de la masse maigre. Autrement dit, l’apport cible n’est pas un chiffre “standard” mais une DER modulée par le niveau de mobilité c’est-à-dire à la masse maigre :
Sur le plan protéique, les besoins sont proches d’un enfant en bonne santé. L’objectif protéique doit être augmenté lors de situations d’hypercatabolisme (chirurgie, escarres, infections prolongées) et associé à une prise en charge globale incluant une amélioration des apports hydriques, des fibres, gestion des reflux... Une intention doit être portée sur l’hydratation4. A cause de l’incapacité à exprimer la soif ou par risque d’inhalation, elle est peut-être sous-évaluée. Une prescription de volume cible et une différenciation des modalités de prises par une adaptabilité des textures peuvent aider4. Les micronutriments sont souvent insuffisants avec, par exemple, une carence martiale dans 54 % des cas. Le calcium et la vitamine D sont à favoriser pour prévenir la fragilité osseuse fréquente chez ces enfants, à cause de leur immobilité et de certains traitements comme des corticoïdes.
4) Quelles stratégies nutritionnelles adopter ?
Le(a) diététicien(ne) est au centre de la prise en charge nutritionnelle de l’enfant atteint de polyhandicap. Sa présence régulière auprès de l’enfant et des aidants est primordiale. Elle permet de confirmer que les apports caloriques sont satisfaisants et que la prise alimentaire est sécuritaire. Une attention toute particulière doit être apportée à la qualité de vie de l’enfant et de sa famille lors des repas. L’alimentation se veut apaisée avec un temps acceptable de moins 3 heures par jour4.
Pour recueillir ces informations, il faut savoir questionner au plus juste les aidants ou le patient s’il peut communiquer. Poser la même question mais de différentes manières consolide les réponses et donc le diagnostic. Le moindre signe d’alerte peut ainsi être dépisté et prévenu.
La figure 2 ci-dessous illustre les différentes réponses de l’audience pendant les DayNutri à Lyon sur la question : « Quels sont les freins l’alimentation que je rencontre chez mes patients ? »

Optimiser la prise orale
quand cela est possible L’objectif de l’optimisation de la prise orale est d’enrichir l’alimentation par des compléments nutritionnels oraux (CNO), d’adapter les textures selon les capacités masticatoires et de déglutition, d’organiser la durée et le rythme des prises (fractionnement, collations) et de favoriser les repas sereins. Les apports caloriques et protéiques sont privilégiés à l’équilibre alimentaire tant que la sécurité et la couverture des besoins ne sont pas obtenues. Les boissons à intérêt nutritif (lait, jus de fruit) permettent d’augmenter les apports caloriques oraux mais doivent être proposés en dehors des temps de repas afin de limiter la surcharge de déglutition.
Choisir sereinement la nutrition entérale
Parfois, malgré tous les efforts, la dénutrition s’installe malgré une complémentation importante en CNO (compléments nutritionnels oraux) et une adaptation des prises alimentaires. Les troubles de déglutition s’aggravent drastiquement et les repas s’éternisent ou épuisent l’enfant4.
Dès ces signaux d’alarme, il est temps de proposer une nutrition entérale. Ce n’est en aucun cas un aveu d’échec mais plutôt une intervention précoce de protection respiratoire et de récupération fonctionnelle. La nutrition orale peut être légèrement conservée pour le plaisir des patients tant que les conditions de sécurité sont conservées4.
Ainsi, trois questions peuvent guider la décision4 : (1) Les apports sont-ils suffisants sur une semaine typique, sans épuiser l’enfant ? (2) La déglutition est-elle sûre ou existe-t-il une suspicion d’aspiration (même silencieuse) ? (3) La charge pour les aidants est-elle soutenable (temps de repas, conflits, nuits fragmentées par le reflux, hospitalisations) ? Si l’une de ces réponses est négative, l’entérale doit être discutée sans attendre.
Concernant l’abord, les boutons sont à privilégier lorsque l’indication est posée. La gastrostomie est l’option la plus fréquente. La gastro-jéjunostomie doit être discutée lorsqu’il existe une nécessité de protection des voies aériennes supérieures, un RGO sévère ou une gastroparésie sévère. Cette hiérarchie est particulièrement pertinente chez l’enfant atteint de polyhandicap où la morbidité respiratoire est un marqueur de gravité.
Le choix des formules dépend de la phase thérapeutique. En renutrition, les formules à privilégier sont les semi-élémentaires ou polymériques, avec options hyperprotéiques ou normoprotidiques, hypercaloriques ou normocaloriques et en association à des fibres. Lors de la phase de maintenance, il faut privilégier les formules polymériques normoprotidiques, normo- ou hypocaloriques, avec un ajout de fibres si cela s’avère nécessaire. La titration des débits et des volumes doit intégrer le reflux, la vidange et la constipation. Lors d’une renutrition efficace, il est nécessaire de veiller à sa tolérance sur le long terme et de ré- évaluer les besoins des patients régulièrement.
Conclusion
Chez l’enfant atteint de polyhandicap, la nutrition doit s’inscrire dans une démarche thérapeutique à la fois préventive et protectrice. La dysphagie souvent silencieuse, les RGO et la constipation doivent alerter notamment sur le risque respiratoire. La qualité de vie et le confort quotidien des patients doivent être surveillés car ils orienteront de nombreux choix et stratégies de nutrition. Les évaluations nutritionnelles doivent être régulières (anthropométrie, composition corporelle, bilans carentiels) et associées à une stratégie réfléchie au domicile. Lorsque cela s’avère nécessaire, une nutrition entérale anticipée permet souvent de rompre la spirale négative des « infections, dénutrition et épuisement ». Toutes les actions menées visent à améliorer le quotidien de ces enfants et de leurs aidants et ainsi, permettre à tous, de vivre une vie plus apaisée et confortable à long-terme.
Bibliographie :
1) HAS, L’accompagnement de la personne polyhandicapée dans sa spécificité. Synthèse, 13 octobre 2020
2) Hamouda I. Thèse de doctorat : La personne polyhandicapée en France : indicateurs de santé, de la performance des soins et de qualité de vie. 15 décembre 2023
3) HAS, L’accompagnement de la personne polyhandicapée dans sa spécificité. Recommandation, 13 octobre 2020
4) DéfiScience – Filières de santé des maladies rares du neurodéveloppement. Protocole national de diagnostic et de soins (PNDS) Générique polyhandicap, 11 mai 2020.
5) Hanna SE et al. Stability and decline in gross motor function among children and youth with cerebral palsy aged 2 to 21 years. Dev Med Child Neurol 2009;51(4):295- 302
6) Leonard M et al. Nutritional status of neurologically impaired children : impact on comorbidity. Arch Pediatr 2020;27(2):95-103
7) Haapala H et al. Agreement between actual height and estimated height using segmental limb lengths for individuals with cerebral palsy. Am J Phys Med Rehabil 2015;94(7):539-546
8) Righini-Grunder F. and Petit Laetitia-Marie. Evaluation de l’état nutritionnel et prise en charge nutritionnelle de l’enfant avec polyhandicap. Paediatrica 2020 ;31 :14-18
Le polyhandicap : 260386 – Mars 2026 - NUTRICIA Nutrition Clinique RCS NANTERRE 451 229 306